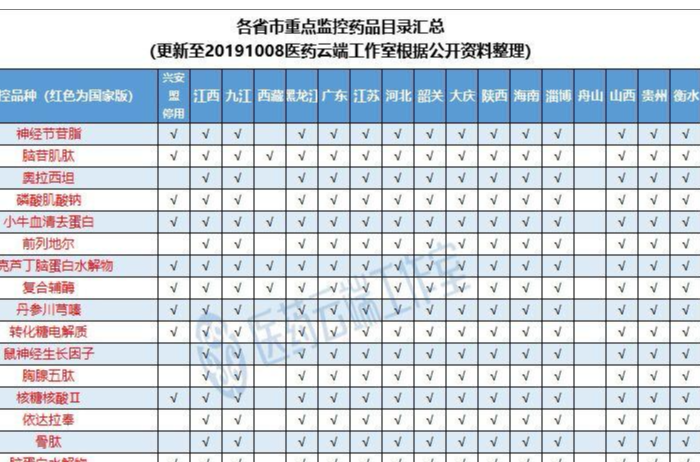
近日,国家药品监督管理局(NMPA)再一次向社会公开《药品注册管理办法(修订草案征求意见稿)》(以下简称《办法》修订稿),吸睛点众多,其中一处重要修改引起笔者注意,同时却发现大家并未太多关注、讨论,笔者抛砖引玉,希望我们在法规颁布前充分讨论、反馈问题。
《办法》修订稿第一章、第五条(药品注册类别)将中药注册分类分为5类:创新药、改良型新药、古代经典名方中药复方制剂、同方类似药、境外已上市境内未上市中药。
中药仿制药去哪儿了?“同方类似药”是什么东东?和中药仿制药有什么异同?研发过程是否与生物类似药一样痛苦?
本次《办法》修订稿中,只有“同方类似药”五个字神一样的存在,没有任何解释和说明,笔者只能另想办法一窥真容了。2017年的《药品注册管理办法(修订稿)》征求意见稿中讲到:“仿制药应当与原研药品或参比制剂质量和疗效一致;生物类似药、同方类似药应当与原研药品或参照药品质量和疗效相当”;再从2017年征求意见稿所附的《中药、天然药物注册分类及申报资料要求(试行)》中找到同方类似药(中药注册4类)的定义:“同方类似药指处方、剂型、日用生药量与已上市销售中药或天然药物相同,且在质量、安全性和有效性方面与该中药或天然药物具有相似性的药品。”
仿制药要达到“一致”相对简单,药学一致、生物等效达到要求基本就可;而类似药要“质量和疗效相当”则难以说清楚,说不清楚的就需要投巨资,做大量的研究,包括大临床试验。做一个生物类似物并不比研发一个生物新药简单多少。
虽然中药注册分类的改变,直接把中药仿制药变成了历史,但也许我国中药研发人员对此已经麻木了,中药仿制药事实上已差不多成为历史。
一个月前,一位朋友想仿制一个中药品种,让药智网做个立项调研报告,我问了一下他的预期和预算之后没有给做调研,直接给出建议:不要仿制了。仿制一个中药仿制药的难度与花费远远大于一个化学药,而且成功的可能性很小。
为何一个中药仿制如此之难,而市场上的中药仿制药又如此之多?让我们先来看看中药仿制药的历史。
在我国历史上“中药仿制药”的批准曾经是很自由、简单的事,特别是在文革期间,药品监督管理被视为管卡压,视为人民用药的枷锁。于是,一个县革委会,或者一个厂长就可以自行“批准”一个药品上市(仿制药如此,新药也如此),直至国务院于1978年7月30日批转了卫生部制订的《药政管理条例(试行)》,条例要求“中西药品生产单位,所生产的每种药品都必须报经省、市、自治区卫生局审核批准”。
当时各省市卫生局下面有个药政处,别看只是省局下面的一个处室,但却拥有批准仿制药品生产的权利,1985年颁布的《药品管理办法》更是用法律的形式规定了:“生产已有国家标准或者省级标准的药品,必须经省级卫生行政部门征求同级药品生产经营主管部门意见后审核批准,并发给批准文号”。
可想而知,当时的中药仿制仍然是轻松+愉快的。基本上只要能找到一个药品的国家标准或省标准,并能生产出三批符合标准的药品,即可批准上市。
仿制中成药,还有一个途径,现在很多人都未曾听说过,叫“中成药移植”。1988年的卫生部发布《关于恢复中成药移植问题的通知》,为了保护一些品种不被滥仿制,1990年卫生部发布《关于加强中成药移植品种的管理通知》,加强规范管理。与简单的仿标准的做法不同,中成药移植单位在本省卫生厅(局)申请移植中成药品种时,必须持有该品种原处方、生产工艺、质量标准及临床研究总结等资料。要想拿到这些资料,可不容易,不过因为当时基本都是国有企业,关系到位,再发扬无产阶级的无私奉献精神,也是可能的。另一个渠道就是很多中成药是科研院所研制成功的,如果合同有疏漏,科研院所就可以“一女二嫁”,将资料卖给另一厂家生产。
这种局面一直维持到1999年国家药品监督管理局(SDA)成立,将地方的药品生产批准权集中到国家药监局,开启了药品监管新篇章。
1985年、1992年、1999年颁布的《新药审批办法》都只讲新药,未将仿制药的审批纳入管理。SDA成立后的2002年,《药品注册管理办法》(试行)颁布,首次将仿制药注册纳入法规体系,中药仿制药成为《办法》中的中药分类的第11类:已有国家标准的中成药和天然药物制剂,对这类药品基本是减免动物试验和临床试验,就是对药学研究的要求也非常宽松。
虽然仿制药的批准权利收归国家药监局,但在2007年以前,中药的仿制注册管理非常宽松,中药处方比较复杂,药物组分繁多,为数不少的研发人员对被仿制药标准不经过分析研究盲目照搬的现象。有的甚至连被仿制药所用药味、处方、工艺等都不清楚就开始仿制。
《药品注册管理办法》掀起了中药厂的仿制热情,从下图我们可以看到中药仿制药快速增加,在2006年达到顶峰(多达2738个受理号,平均每个工作日受理10个以上)。
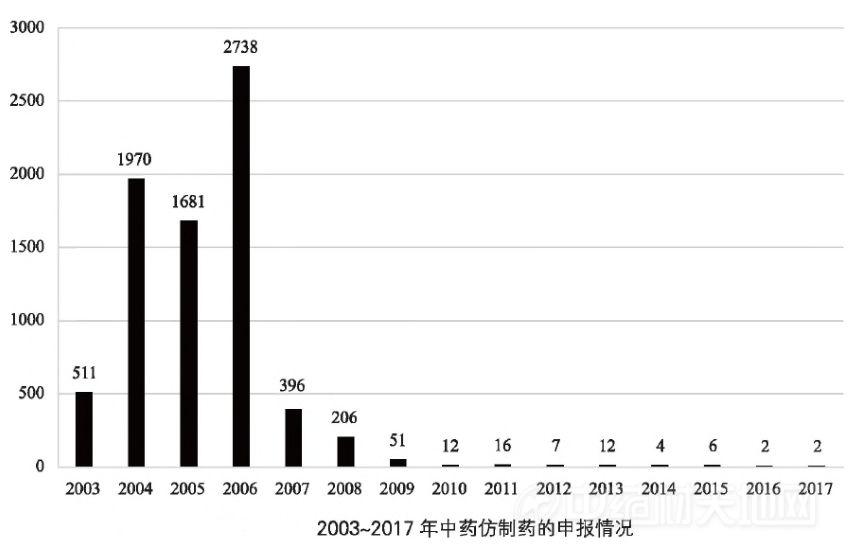
图片来源《中国医药研发40年大数据》
虽然存在这么多的问题,但客观上,在药品供应侧还是卓有成效,那就是让众多的独家品种、准独家品种(生产厂家很少)有了较多的仿制药,或者是剂型不同的相同品种。一旦有了仿制药这个竞争对手,高高在上的药价就低下了高贵的头。所以从这个意义上讲医保部门应当感谢那个天天有中药仿制药获批的年代。但受益于国家技术秘密品种、中药保密品种、中药保护品种、标准未转正不得仿制等等特色法规,还是大量的独家品种孤独至今。
疯狂之后便是幻灭,从上图可看看到,在2006年药品注册核查,2007年新《药品注册管理办法》出台后,中药仿制药的申报出现断崖式的下降,从此一蹶不振,至今已是“苟延残喘”,每年只有几个仿制药申报。下图中注册9类(绿色)即为中药仿制药在2008年占比成为第一后即呈下降趋势,近几年每年中药仿制药的申报数量竟然远小于中药新药(临床、上市)申报数量,可见中药仿制有多难,难于做新药?!

说明:注册9类(绿色)为中药仿制药,注册6类(黄色)为复方新药
2007年以后,SFDA加强了中药仿制药的管理注册,仿制药要求按照被仿制药的药材(基源)、处方、工艺进行研发、生产,而这等详细信息难以合法获取,而且视却只是临床批件,想着还需要巨额的临床投入与承担临床失败的巨大风险,老板只好默默地将临床批件锁在档案室。情况需要开展临床试验,大大提高了中药仿制难度。曾经有不少企业试图闯关,但不是多次发补,就是不批准,有的拿到了批件,
仿制药申报比新药申报数量还少,也算是一大奇观吧,是否是政策导向存在一定问题?仅就技术层面而言,严格把关,不让疗效得不到保障的药物进入市场,这是对的。比如因为原研的A药未曾经过系统的新药临床试验验证,有效性值得怀疑,就大大提高A药的仿制药上市门槛。可是换一个思路,因为没有A药仿制药,该药作为独家品种,以高昂价格进入医保,在中国特有的医药市场上大卖特卖,与其这样,还不如批准其仿制药,至少医保和患者少支出了,经过数年的竞争,也许这个品种的市场占有量反而就变得很小了。
近10年来仿制药申报数量太少,获批者更少,导致独家、准独家中药处于垄断、半垄断地位,中药价格长年居高不下。一些中药企业老总一方面埋怨这个“近乎不能仿制”的仿制药政策,一方面却也偷着乐:“这个政策捆住了自家的手,也捆住了竞争对手,我家的这些独家品种虽然没有专利,却享受了比专利更长的独家占有权,也许还会保持50年不变”。
穷则思变,但变了是否就通,则要考量智慧。如果要根本性解决问题,就是进行严格的药品再评价。不过基于现状,这根本不可能,即使是中药注射剂的再评价政策也是千呼万唤不出来。目前关于中药仿制药的变化在于两方面:
一是出台了“古代经典名方中药复方制剂”相关政策,中医药管理局出台了首批经典名方100首,其中约有10首方剂与已上市产品处方相同,悄悄的推开了一扇门。可惜国家药监局出台的文件规定现有上市品种不能按“经典名方制剂”注册申报,又悄无声息地关上了中药“仿制”的这扇侧门,缺少“大品种”的诱惑,厂家申报积极性并不高。希望在《药品注册管理办法》修订后加以调整,放开此条限制,让独家品种有类似的竞品竞争。也算是在仿制药受“堵”的同时给个“疏”的通道。
另一变化,则是本文开篇提到的将中药仿制药取消,变成同方类似药。听名称、观定义,同方类似药的申 报难度更甚于中药仿制药,如果真是按生物类似药的思路,要求同方类似药进行临床试验的话,这就是座难以逾越的高山。要讲特色,我倒认为同方类似药可以充分考虑中医药特色,在随后出台的具体细则、指导办法中为中药的仿制打开一道小小的门,让门内的独家中药品种不再一直“孤独”。
(本文转载自其他网站,不代表中药材天地网的观点和立场。如有著作权异议请及时联系我们)