下拉刷新
加载中...
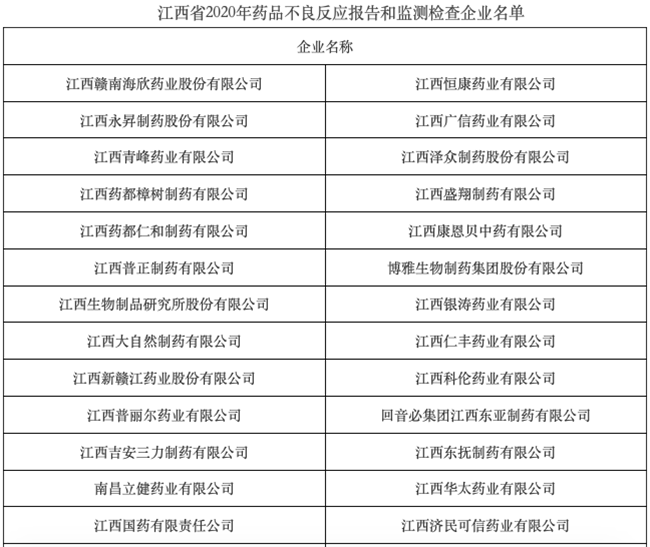
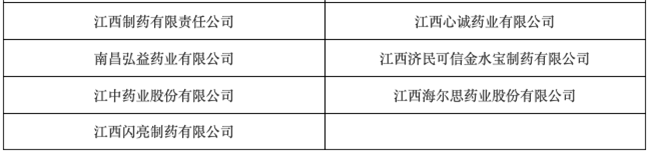
药监局最新通知 33家药企被点名
2020-09-08 11:02:00
推荐资讯
-
舆情监测
26批次药品被查不合格(附名单)
2020-09-08 09:41
-
舆情监测
曝光:11批次药品不合格被通报
2020-09-03 14:40
-
舆情监测 厦门海关破获亿元茯苓走私大案2020-08-31 13:45

-
舆情监测 刚刚:11批药品(9批中药饮片)抽检不合格,五灵脂等6批因性状,地龙(检查项)!2020-08-28 14:25
-
舆情监测
国家药监局:13种药停售、召回
2020-08-26 16:04
热门资讯
-
舆情监测
重点检查中药饮片市场 筑牢群众用药安全屏障
2026-04-10 14:24
-
舆情监测
货值0.45万,被罚50万!中医诊所采购中药饮片最容易踩的“雷区”
2026-04-21 15:40
-
舆情监测
天目药业被警示,因信息披露不准确
2026-04-21 16:10
上拉刷新
加载中...
正在加载