下拉刷新
加载中...
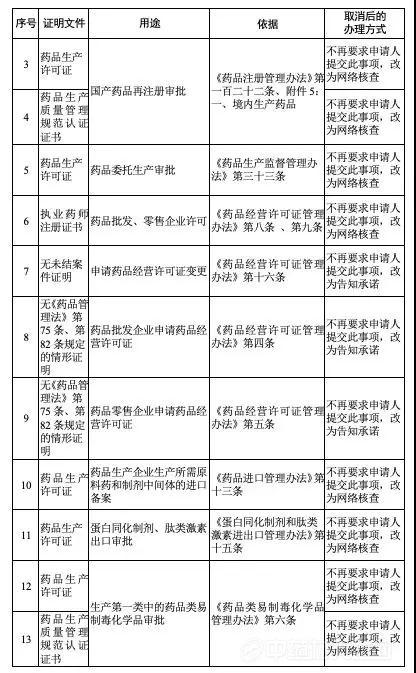
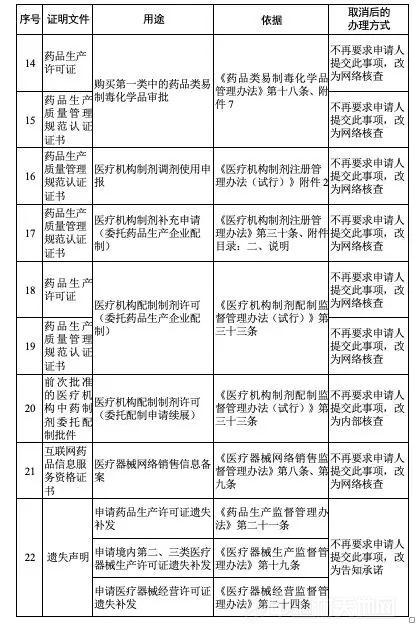
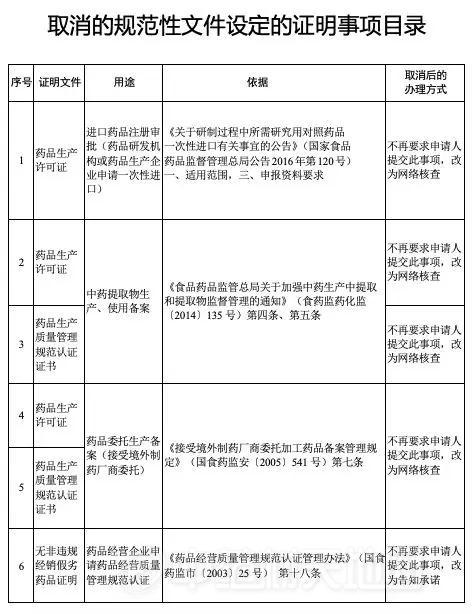
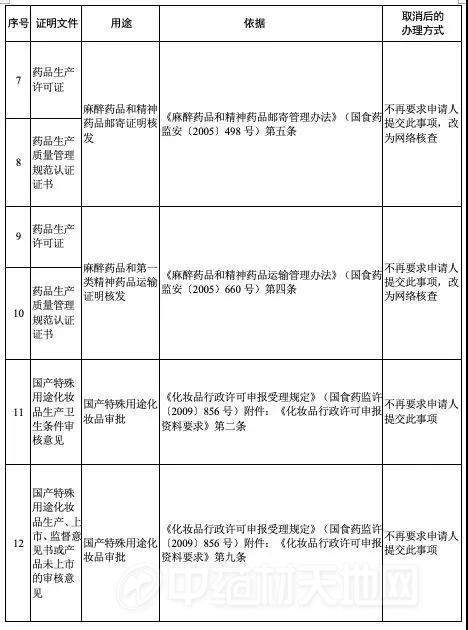
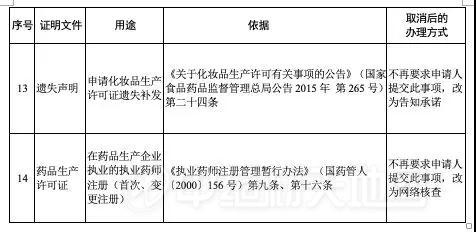
国药监局:办理这36项,再也不用提交药品生产许可证、GMP证了!
2019-04-29 11:50:17
推荐资讯
-
政策解读 警示!全国药店大整治 14条红线别踩2019-04-29 11:12

-
政策解读 中国人大网:《药品管理法(修订草案)》全文2019-04-28 10:15

-
政策解读 最新文件公布 涉所有药企药商2019-04-26 16:41

-
政策解读 国家药典委:拟修订巴仙苁蓉强肾胶囊、肠胃宁胶囊、刺五加脑灵胶囊、刺五加颗粒国家药品标准2019-04-26 14:55

-
政策解读
4+7带量采购落选 企业如何争取市场份额
2019-04-25 17:42
热门资讯
-
政策解读 《中药工业高质量发展实施方案(2026—2030年)》解读2026-05-09 10:09

-
政策解读 反腐、严管、优质优价 ——中药饮片行业三大变局,基层诊所如何应对?2026-05-14 10:25

-
政策解读 中华人民共和国药品管理法实施条例2026-05-15 11:03
上拉刷新
加载中...
正在加载