下拉刷新
加载中...
国家市场监督管理总局发布《进口药材管理办法》,溯源管理成为重点
2019-06-11 16:40:58
推荐资讯
-
政策解读
七部门印发《肉菜、中药材等重要产品追溯体系建设的意见》,标准不一难成中药产品挡箭牌
2019-06-11 16:19
-
政策解读 两部门对药企“穿透式”查账 谁会倒下?2019-06-11 16:17
-
政策解读 2019年河北省中药材产业发展指导意见,涉及安国有哪些?2019-06-11 15:15

-
政策解读
教育部印发2019年中医学、民族医学免费本科医学生招生培养,医学类专业再成高考填报热门
2019-06-11 11:17
-
政策解读
注意这些人,未来两年,医保个人账户将取消?
2019-06-06 11:26
热门资讯
-
政策解读 《福建省规范中药材产地加工(趁鲜切制)指导意见》政策解读2026-02-26 14:57
-
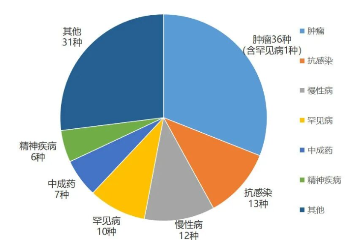
政策解读 中药产业大爆发!创新驶入快车道,医保加大支持,推进新集采……趋势解读2026-03-04 11:08
-
政策解读
2026年中药材产业的“分水岭”:要么成为“规范玩家”,要么被“集采红利”清场!!
2026-03-04 10:50
-
政策解读
学习2026年中央一号文件:关于粮经产业和农业科技创新、中药材等相关内容
2026-03-04 10:46
-
政策解读
《中医药继续教育管理办法(试行)》政策解读
2026-02-28 10:54
-
政策解读 学习2026年中央一号文件:关于粮经产业和农业科技创新、中药材等相关内容2026-03-04 10:44

上拉刷新
加载中...
正在加载



