下拉刷新
加载中...
好消息!陕西药品GMP认证工作日由145个压缩至63个
2019-06-28 10:09:07
推荐资讯
-
政策解读
4+7后,药企都在布局这一市场
2019-06-27 17:05
-
政策解读
《安徽省中医药条例(草案征求意见稿)》,就中医药问题向公众征求意见
2019-06-26 11:55
-
政策解读
辅助用药目录将出 大品种如何寻找再次进入临床使用的出路
2019-06-25 17:34
-
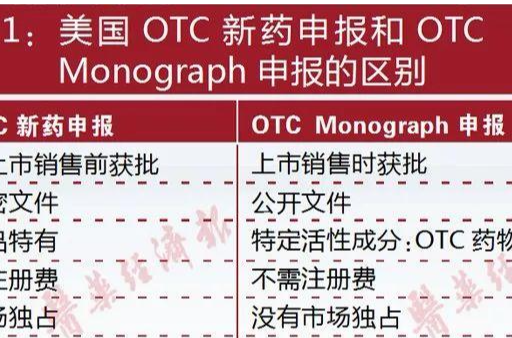
政策解读 医院市场承压!转战OTC,药企必看攻略2019-06-25 14:14
-
政策解读 中医管理局严控中药饮片大处方和超量使用,将影响3500亿中药饮片市场?2019-06-24 15:45

热门资讯
-
政策解读 国新办举行国务院政策例行吹风会介绍健全全周期全渠道药品价格形成机制有关情况2026-04-16 10:34

-
政策解读
国务院关于产业链供应链安全的规定
2026-04-08 10:16
上拉刷新
加载中...
正在加载



