【天地网讯】
1月25日,国家药监局网站公布了甘肃博祥药业、天水康泰药业、华润西安医药、达州市朝阳医药、娄底民康医药、合肥顿克生物医药、鸡西市辰曦药业7家医药企业的飞行检查通报,并给予撤销企业GSP认证证书的处理措施。具体的通报情况如下:
对甘肃博祥药业有限公司飞行检查通报


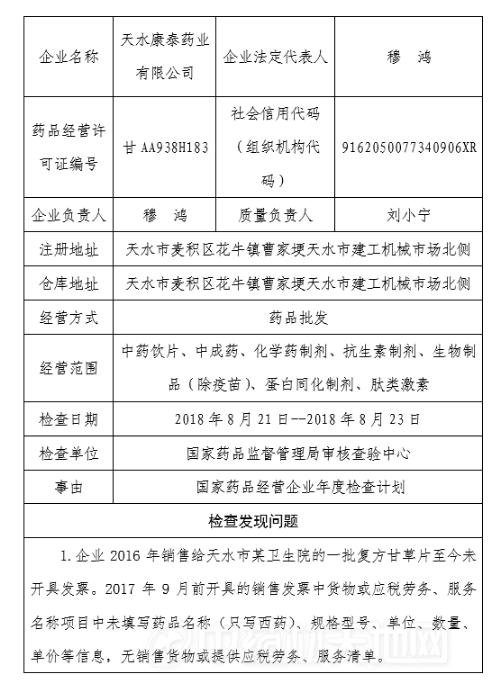
对天水康泰药业有限公司飞行检查通报

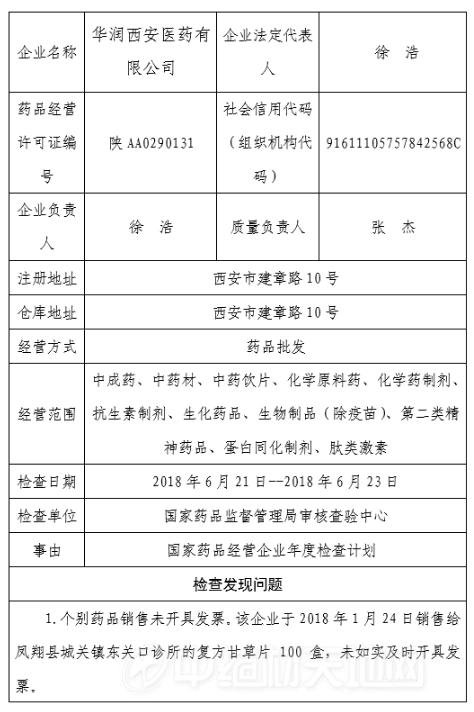
对华润西安医药有限公司飞行检查通报

对达州市朝阳医药有限责任公司飞行检查通报


对娄底民康医药有限公司飞行检查通报



对合肥顿克生物医药有限公司飞行检查通报


对鸡西市辰曦药业有限公司飞行检查通报



2018年自4月以来,撤证企业数明显增加。在接近农历新年,国家药监局官网更是频繁贴出处罚通告,显现出2019年飞检会持续升温。虽然大部分医药企业都是兢兢业业按照国家规定履行企业职责。但是,尤其是在临近新年期间,总会有一丝疏漏。一个措手不及,就会面临收回或者撤销GSP认证的局面。
面对监管不断加强的形式,药企该怎么办?飞行检查的要点和重点有哪些?听听国家级GSP检查员怎么说?
违法行为及重点检查内容
1经营主体违法行为分类及检查依据
无证经营及超范围经营,《药品管理法》第14条。
不具备经营条件,《药品管理法》第15条。
不符合药品GSP规范,《药品管理法》第16条。
购销假劣药品,《药品管理法》第48、49条。
从非法渠道购进药品,《药品管理法》第34条。
伪造、出租药品经营许可证照,《药品管理法》第82条。
经营没有进口注册证药品,《药品管理法》第39条。
其它:医院制剂、赠送药品、私设仓库等。
2飞行检查内容
分工协作,根据企业特点开展针对性检查;
向企业索取购销流向数据、财务凭证、人员名称和首营资料等;
做好证据收集、取证工作;
对空调系统温湿度及报警系统进行检查;
抽取代表性样品,对其首营资料与电脑记录情况比对;
对电脑系统登录账号密码管理、权限设置及登录日志进行检查;
对电脑上的QQ、微信及硬盘数据进行检查;
对购销存系统抽样品种销售额与发票数量进行比对;
对财务凭证、预付、应付款白条及购销发票进行检查;
对中药材收购和销售情况进行检查;
对特殊药品、冷链药品进行检查;
对可疑情况,开展上下游延伸检查。
3检查步骤及要点
固定证据、堵住后路
检查组分工协作,同时取证
堵住后路:检查员A负责对仓库进行检查,要求仓库保管员对进销存时间段内的流水打印或U盘备份,并进行确认,重点检查发货区、收货区、退货区域内各种票据及货物,对仓库操作区内办公台、计算机等进行重点检查,查找证据;检查员B负责对财务部门进行检查,重点检查财务部办公台、保险柜、快递信封等在内的各种来往票据进行收集,要求将时间段内记账凭证等全部搬至检查组会议室;检查员C负责对质量部门办公室进行检查,要求质量负责人将企业员工花名册、聘用合同、培训资料及关联交易全部企业及药品首营资料搬到检查组会议室。
再次与企业负责人确认,上述资料是否为企业全部真实材料?
a检查关键要点1:现场收集证据
收集各种现场票据,对仓库收发货区、财务部、销售部及经理办公室等经营场所进行细致检查;
对快递信封、保险柜、文件柜依法依程序进行检查,收集涉及规范的证据;
对经营场所电脑QQ、微信对话及系统贮存的各种证据进行取证;
对企业营业场所、仓库的录像进行取证;
对空调系统运行、报警及记录进行取证;
对质量管理部及负责人场所进行检查;
对经营场所面积、楼上楼下观察是否有私设仓库。
b检查关键要点2:现场药品抽查样品
对特殊管理药品进行取样核查;
对退货药品进行取样核查;
对冷链药品进行取样核查;
对违反常理或可疑药品取样进行核查;
对含毒性成分的中药饮片和中药材取样核查;
对控销、进口抗肿瘤、心血管、血糖类药品取样;
对违反先进先出及采购近效期的药品取样核查;
对购销发票数据最大的药品进行核查。
c检查关键要点3:账务记账凭证的核查
购进与销售金额的平衡核查;
企业仓库规模与销售数量的平衡核查;
对预付款或应收款白条的核查;
对采购数量特别大或发票金额特别大药品的核查;
对销售到个体诊所、药店是否开具发票;
对特殊管理药品销售是否现金交易;
重点核查现金交易,企业名称、资金流向是否一致;
对集团企业开办的药品批发重点查进出项发票异常情况,对中药材收购发票进行针对性核查,购销流向真实性。
d检查关键要点4:询问笔录
对药品经营企业购销、管理人员询问笔录,发现违规线索;
坚持从低层往高层,仓管、财务再到质量、销售、经理询问原则;
注重询问策略和技巧,聊天、引导和压迫相结合;
单独、分开原则,避免串口供;
询问笔录可交当地药监部门完成;
抓住一条线,一直往前追,避免多点出击。
4检查要点:直接查找现场违规行为(批发)
检查仓库区内各种可疑行为:
是否经营假劣药品;
是否分装、加工中药饮片;
是否设置非核准仓库;
库房温湿度、控制空调系统温湿度、报警系统是否正常;
对退货区的药品及退货操作进行检查;
对特殊药品进行重点检查;
对仓库区内的票据、运输单据进行收集;
对库房面积、经营规模、存货及仓库管理情况等进行初步评估。
5检查要点:直接查找现场违规行为(零售)
检查药店及周边内各种可疑行为:
是否经营假劣药品,特别是柜台底下、工作间内药品;
是否分装、加工中药饮片行为;
是否设置非核准仓库;
药店内冰箱温湿度、空调系统温湿度是否正常;
对退货药品及退货记录进行检查;
对特殊、拆零药品进行重点检查;
对药店的各种票据进行收集;
对药店经营规模、存货及仓库管理情况等进行初步评估。
6从哪些地方发现问题?
从企业成本核算入手,成本最高的地方往往是违法违规。
从企业生产经营规模与实际能力比较。
从企业文化入手,企业核心价值观是什么?
从企业从业者入手,员工的能力、执行力等反映是否规范。
从企业经营诚信体系入手,诚信是企业之本。
从企业经营合作对象入手,上下游联动核查。
依靠电子监管、网络媒体等查找企业关联信息。
现场检查中常见的问题及成因
质量管理体系不完善
目前企业的质量管理文件系统普遍存在着一个问题:企业制定文件中的规定与实际情况不相符。文件中制度、职责、操作规程不够具体,关键性的内容缺失,使得文件缺乏可操作性,从而导致企业无法准确把握文件的关键内容,各岗位人员职责不清,日常质量管理工作未按规定程序完成。
人员素质有待提高,部分企业对从业人员的管理不重视
对人员资质不重视,相当一部分企业的从业人员大多数是高中学历,人员素质起点较低。
人员培训和继续教育不重视,企业未定期开展内部培训,人员上岗培训走过场。尤其是对新增计算机系统的操作培训、冷藏冷链设备的应急培训存在较大的欠缺。缺陷项目的统计表明,有一半以上的企业的人员培训不到位。
关键专业人员未在职在岗。部分企业的质量负责人及质量管理人员经常缺勤或兼职,甚至挂靠,未对企业进行质量管理指导和员工培训,未组织开展质量管理活动,导致质量管理体系形同虚设。
硬件配备欠缺
一些企业质量管理意识不强,把药品存储区、作业区和办公区等混合在一起,仓库的地面、墙面不光洁、不平整,门禁系统缺失,库房门窗结构不严密,避光通风设施不足,防虫、防鼠、防火设备老旧,经营中药材不配备中药标本室、养护室等。
尤其是新修订GSP要求较高的设施设备,如温湿度调控及自动监测设备、冷藏冷链设施设备、计算机等等,企业或因出于节约成本考虑或因对新修订GSP设施设备要求认识不到位,导致这类硬件设备无法满足经营的需要,无法达到新修订GSP的要求。而且很多企业对所使用的设施设备未定期进行检查、维修、养护,没有操作记录或记录不完善,设施设备档案内容不齐全。
过程控制不健全。
新修订GSP要求企业的整个业务流程都能用计算机系统控制。然而很多企业的计算机系统仍存在这样那样的问题,如权限设置的不合理、基础数据库的不完善、部分功能模块的缺失、操作人员的不熟练等等。在药品的购进与验收环节,部分企业未编制药品购进计划,或编制的药品购进计划不以药品的质量为重要依据,也无质量管理机构人员参加;向供货商购进药品未与供货商签订有效的购货合同或质量保证协议;对进货情况未按要求进行质量评审,药品验收未按要求抽取样品;药品的验收未做到逐批开箱验收或未按验收规程要求进行验收。
在药品的储存与养护环节,部分企业未对验收养护用器具定期进行检定,发现可疑药品未及时锁定;药品储存不按分类要求集中堆放;在库药品未定期进行检查和养护,或未建立药品的养护档案;不汇总分析上报养护药品质量信息等等。
在药品的出库与运输环节,部分企业不按“先产先出、近期先出、按批号发货”原则进行发货;药品出库复核记录不按要求保存;药品运输未按药品的要求来取相应的措施等等。在药品销售与售后服务环节,部分企业对售出药品的不良反应情况未收集也不上报等。
资料来源:国家药监局网站、CIO合规保证组织
声明:本文是中药材天地网原创资讯,享有著作权及相关知识产权,未经本网协议授权,任何媒体、网站、个人不得转载、链接或其他方式进行发布;经本网协议授权的转载或引用,必须注明“来源:中药材天地网(www.zyctd.com)”。违者本网将依法追究法律责任。