下拉刷新
加载中...
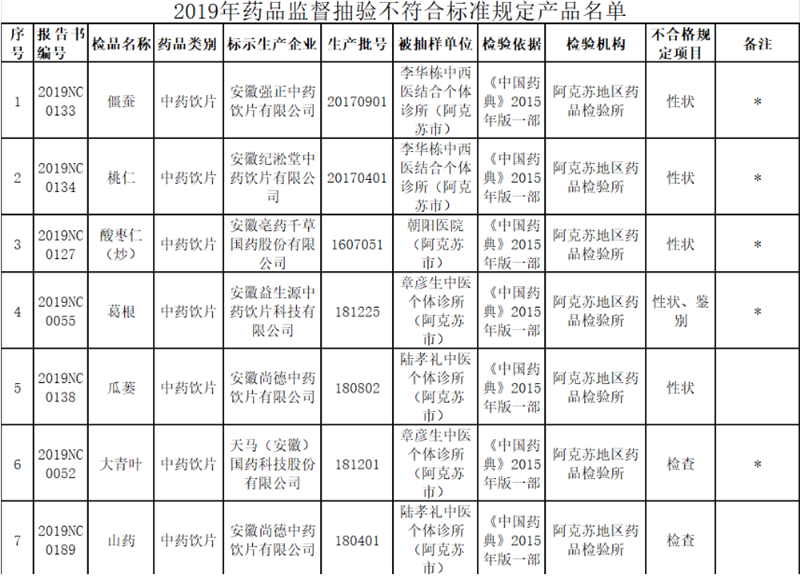
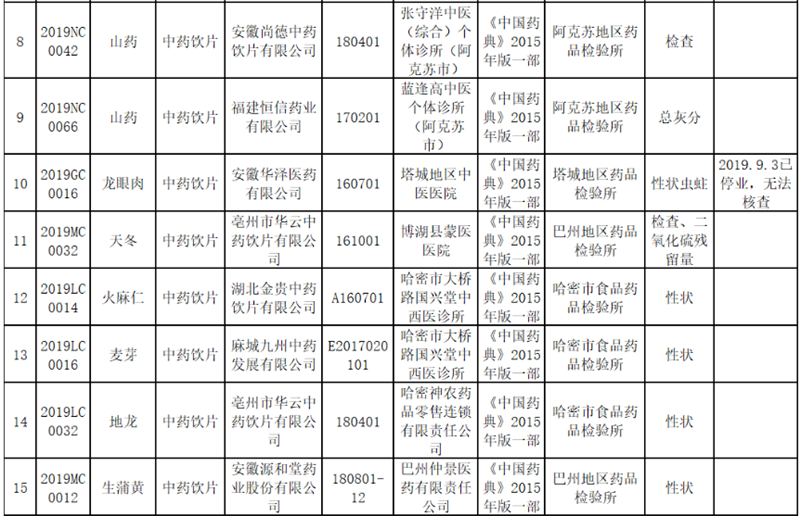
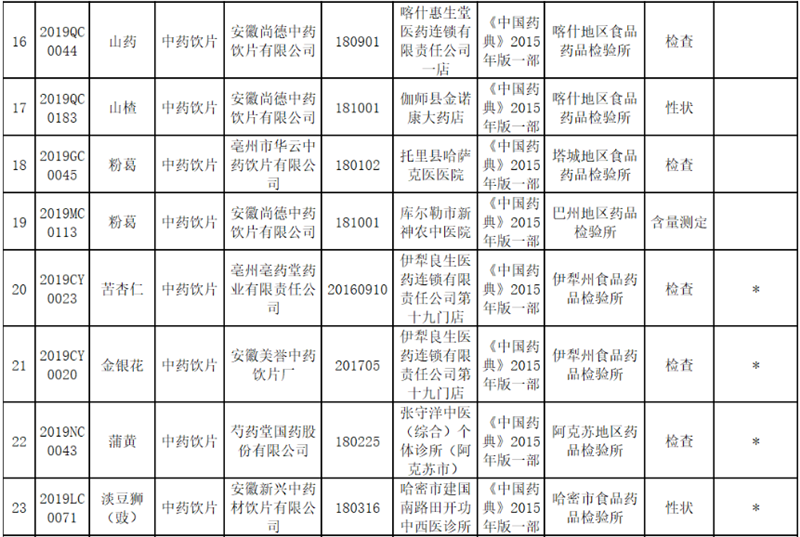
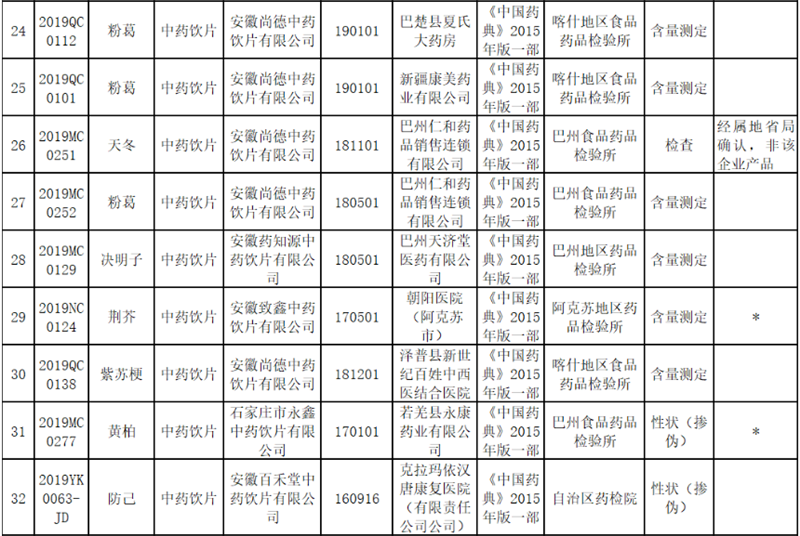
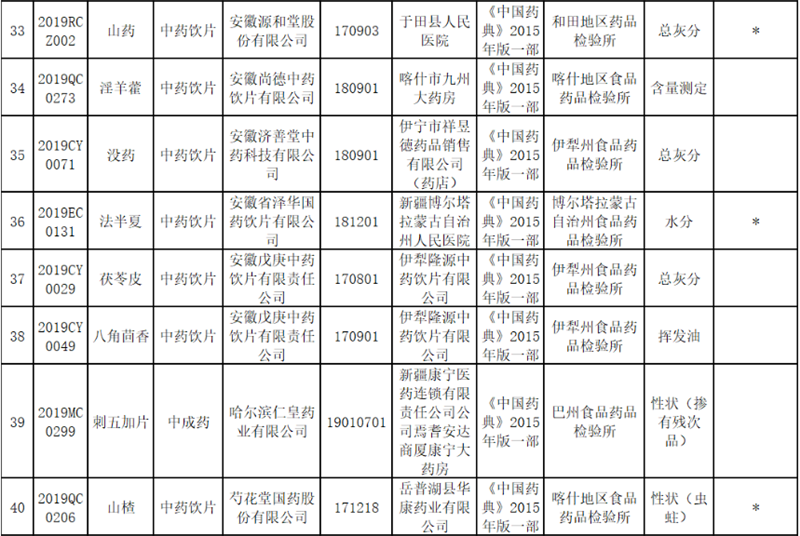
【违法通报】新疆药监局发布饮片质量公告 这5种情形无需检验直接定性假药、劣药
2020-05-14 15:18:32
推荐资讯
-
舆情监测
【违法通报】宁夏多家公司销售劣药饮片被罚
2020-05-12 15:52
-
舆情监测
【违法通报】上海德大堂国药有限公司4批次中药饮片抽检不合格
2020-05-12 14:16
-
舆情监测
【违法通报】山东药监局:七批次饮片不合格 多为性状不符
2020-05-12 11:48
-
舆情监测
【行业乱象】骗取68名药商近300万元中药材 女子领刑十一年半
2020-05-11 11:26
-
舆情监测 【违法通报】河南省药监局通告15批次药品抽检不合格2020-05-08 15:59
热门资讯
-
舆情监测
货值0.45万,被罚50万!中医诊所采购中药饮片最容易踩的“雷区”
2026-04-21 15:40
-
舆情监测
天目药业被警示,因信息披露不准确
2026-04-21 16:10
-
舆情监测 广西1家企业因生产劣药续断被行政处罚!2026-05-13 13:32
-
舆情监测 北京共检查出2家企业GMP不符合规定!2026-05-13 13:35
-
舆情监测 国家医保局关于公开发布第十一批智能监管“两库”规则和知识点的公告2026-05-11 14:26
上拉刷新
加载中...
正在加载